O transporte de oxigênio no sangue ocorre sob duas maneiras:
Dissolvido no plasma e no fluido intracelular eritrocitário. Além disso combinado quimicamente de modo reversível com a hemoglobina.
Transporte de Oxigênio Dissolvido
Quando o oxigênio se difunde dos alvéolos para o sangue, quase todo ele vai penetrar nas hemácias. Desse modo que se combina à hemoglobina. Apenas uma pequena porção permanece no plasma e no fluido intracelular eritrocitário. Além do mais de ser transportada para os tecidos em solução simples. Sendo este é o denominado oxigênio dissolvido, também dito oxigênio em solução física. Desse modo de transporte obedece à lei de Henry, antes descrita.
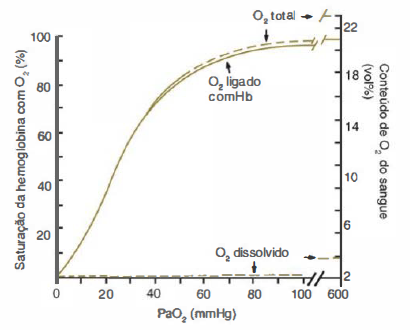
Sendo assim, a quantidade de oxigênio dissolvido é diretamente proporcional à sua pressão parcial no sangue. Para cada mmHg de Po2, há 0,003 mf de 02/100 mf de sangue (frequentemente expresso como 0,003 vol%). Logo, no sangue arterial normal (considerando-se a Po2 igual a 100 mmHg) existe somente 0,3 vol% de oxigênio dissolvido (Figura 44.4). Quando um indivíduo hígido respira 02 puro ao nível do mar, a Po2 eleva-se para um máximo teórico de 673 mmHg, a Po2 arterial excede 600 mmHg e
seu 02 dissolvido se aproxima de 2 vol%.
Por outro lado, as câmaras hiperbáricas aumentam a pressão total para valores muitas vezes acima da pressão atmosférica. Por conseguinte, durante a oxigenação hiperbárica a concentração de 02 dissolvido aumenta proporcionalmente de acordo com a lei de Henry e passa, assmi , a representar uma significativa fração da quantidade total de 02 transportado no sangue. Portanto alguém que respirasse oxigênio puro sob pressão de três atmosferas teria uma Po2 alveolar de cerca de 2.000 mmHg, e seu sangue
arterial conteria aproximadamente 6 vol% de 02 dissolvido.
O oxigênio em altas concentrações é, todavia, extremamente tóxico, podendo levar à morte. Consequentemente, a administração de 02 deve sempre ser feita sob criteriosa supervisão médica.
Transporte de Oxigênio combinado com a hemoglobina
A quantidade de 02 dissolvida não é, entretanto, suficiente para manter funcionante o organismo de um indivíduo normal. No repouso, mais de 95% do oxigênio fornecido aos tecidos são transportados em associação com a hemoglobina, e este valor ultrapassa 99% durante exercício físico. Desse modo cerca de um terço do volume da hemácia corresponde à hemoglobina.
A porção polipeptídica da molécula da hemoglobina normal do adulto (HbA) é composta por quatro cadeias de aminoácidos: duas cadeias alfa (cada uma constituída por 141 resíduos de aminoácidos) e duas beta (cada uma formada por 146 resíduos de aminoácidos). Sendo assim, a sequência desses aminoácidos é extremamente importante para determinaras propriedades da hemoglobina.
Transportes das hemoglobinas
Um outro exemplo pode ser dado pelas hemoglobinas anormais. Atualmente, já são conhecidas mais de 30 hemoglobinas anormais, que chegam a diferir da HbA por apenas um único aminoácido na cadeia alfa ou beta. Amais conhecida é a HbS, presente nos pacientes portadores dea nemia falciforme, um distúrbio de origem genética.
A doença recebeu esse nome porque a hemácia adquire a forma de foice quando a hemoglobina se desoxigena e, anormalmente, se cristaliza. Além do mais das quatro cadeias polipeptídicas, a hemoglobina apresenta um grupamento heme ligado a cada uma das quatrocadeias. Esse grupamento é um complexo constituído por uma protoporfirina e um íon ferro no estado ferroso.
A esse íon,associa-se o 02 quando de seu transporte, formando a oxi hemoglobina(HbO:z). Também nesse ponto se liga o monóxido de carbono (CO), compondo a carboxi-hemoglobina(HbCO). A afinidade da hemoglobina pelo CO é cerca de 200a 300 vezes maior que pelo 02. Desse modo resulta daí que a intoxicação pelo CO (fumaça de cigarro, gases eliminados por motor nessa explosão, gás para uso domiciliar e outras fontes menos importantes) é extremamente grave. Portanto o CO ocupa o heme,
impedindo a ligação do 02•.
Papel do Ferro
Também o estado do íon ferro tem grande importância para o transporte de oxigênio. Caso o
ferro se encontre oxidado, isto é, no estado férrico, forma-se a metemoglobina, que se combina com numerosos ânions, mas não com o 02•.
Ela é produzida na intoxicação pelo nitrito e nas reações tóxicas a medicamentos oxidantes. Também há uma forma congênita de metemoglobinemia, decorrente de uma deficiência da enzima metemoglobina redutase, que reduz o ferro férrico a ferroso.
Cada molécula de hemoglobina, portanto, tem capacidade transportar no máximo quatro moléculas de 02•. Logo, expressa-se em g% a quantidade de hemoglobina no sangue. Desse modo em um indivíduo
hígido, a taxa dessa proteína é de aproximadamente 15 g% (15 g de hemoglobina em 100 mR de sangue). Sendo assim, sabe-se, também, que 1 g de hemoglobina é capaz de fixar 1,39 mR de 02.
Determinação das taxas
Assim, determinando-se a taxa de hemoglobina de um indivíduo e multiplicando-se esse valor por 1,39, tem-se sua capacidade de oxigênio (abreviadamente: capacidade), ou seja, se a hemoglobina estiver completamente saturada por oxigênio. Desse modo o sangue será capaz de transportar Hb (g%) X 1,39 vol% de 02•. A quantidade de 02 realmente associada à hemoglobina depende do valor do 02 dissolvido, visto que a oxigenação é um processo reversível dependente da Po2 a que está exposta a hemoglobina. A relação (Hb02 X 100)/Hb total é chamada de porcentagem de saturação da hemoglobina (abreviadamente: saturação, S02).
É uma maneira prática de expressar o nível de oxigenação de uma amostra sanguínea, independentemente da taxa de hemoglobina. Desse modo, a quantidade total de 02 transportada pelo sangue denomina-se conteúdo de oxigênio. Abreviadamente, o conteúdo e corresponde à soma da quantidade dissolvida com a ligada à hemoglobina.
Diferentemente do 02 dissolvido, a quantidade de oxigênio combinada com a hemoglobina não está linearmente relacionada com a Po2, mas descreve-se sobre ela como sendo uma curva sigmoide (em forma de S). Colocando-se, em um gráfico, no eixo das ordenadas a saturação (ou o conteúdo de Oi) e no eixo das abscissas a Po2, observa-se o aspecto peculiar da curva de equilíbrio entre Hb e 02, também chamada de curva de dissociação da hemoglobina.
A curva de dissociação da hemoglobina é consideravelmente íngreme no seu trecho inicial até cerca de 40 ou 50 mmHg de Po2, enquanto a porção final gradualmente se horizontaliza. Na parte ascendente, as variações de S02 são quase proporcionais às de Po2, ao passo que, na parte alta da curva, grandes modificações de Po2 correspondem a pequenas variações de S02.
Fatores que modificam transporte e o equilíbrio do oxigênio
com a hemoglobina
Há quatro fatores bem conhecidos que alteram a interação do 02 com a hemoglobina: Pco2, pH, temperatura, e nível do 2,3-difosfoglicerato. Observa-se que o aumento da Pco2 desloca para a direita a curva de dissociação da hemoglobina, reduzindo a afinidade da hemoglobina pelo 02. Do
mesmo modo, a elevação da concentração dos íons hidrogênio. Ou seja, a queda do pH sanguíneo, também desloca para a direita a curva.
Sendo assim, essa alteração na posição da curva decorre da modificação na forma da molécula de Hb, o que dificulta a ligação do oxigênio ao complexo heme. A esses dois fenômenos, denomina-se efeito Bohr. À medida que o pH cai e a curva se desvia para a direita, a saturação da Hb para uma dada Po2 decai.
Contrariamente, a elevação do pH desvia a curva para a esquerda, e a saturação de Hb para uma dada Po2 aumenta, indicando maior afinidade da Hb pelo oxigênio. Variações na temperatura também afetam a curva de dissociação de Hb. Enquanto a queda da temperatura redunda em desvio da curva para a esquerda, a temperatura elevada desvia a curva para a direita. O 2,3-difosfoglicerato
(2,3-DPG) é um produto intermediário constituído durante a glicólise anaeróbia, via energética da hemácia.
Hipoxemia e anemia aumentam a concentração intracelular de 2,3-DPG. Quando a concentração de 2,3-DPG se eleva no interior da hemácia, a curva de equilíbrio entre o 02 e a hemoglobina desloca-se para a direita.